大腸癌化学療法
1. 術後補助化学療法
術後補助化学療法とは、目に見える癌は切除した患者さん(治癒切除例)に対して、再発を抑制し予後を改善する目的で、術後に実施される化学療法です。
術後補助化学療法を行うことが推奨されるのは、主として再発の可能性が高いステージⅢの患者さんです。
また、ステージⅡの患者さんであっても、再発の可能性が高いと判断される場合には、術後補助化学療法を行う場合があります。

当院の化学療法専用の部屋です.
大きな椅子でテレビ鑑賞もできます.
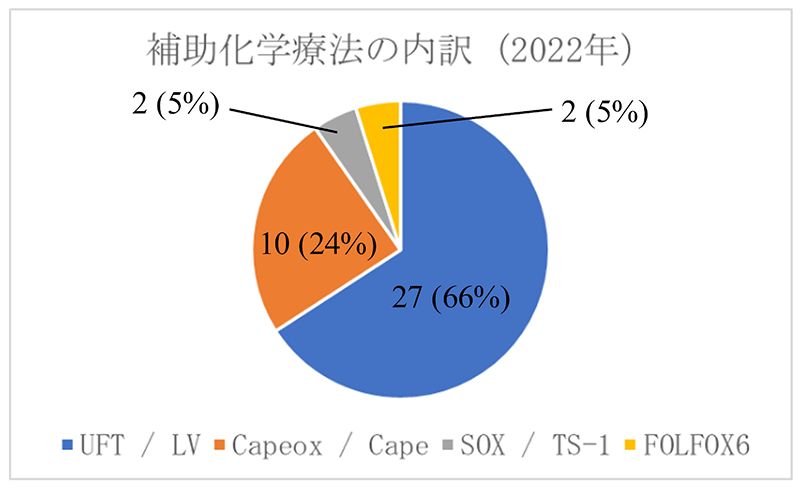
保険適用されている術後補助化学療法には、以下の治療法があります。
使用する薬の種類や量が異なりますが、通常は約6カ月間行います。
からだの状態や副作用の程度によっては、薬の量を途中で変更することもあります。
- 1.UFT+LV療法
- 2.カペシタビン療法
- 3.カペシタビン+オキサリプラチン療法(CapeOx療法)
- 4.FOLFOX6療法
1・2は内服薬のみですが3・4は内服薬に加えて点滴薬が必要です。
当科では昨年は大腸癌術後補助化学療法を年間53例行いました。
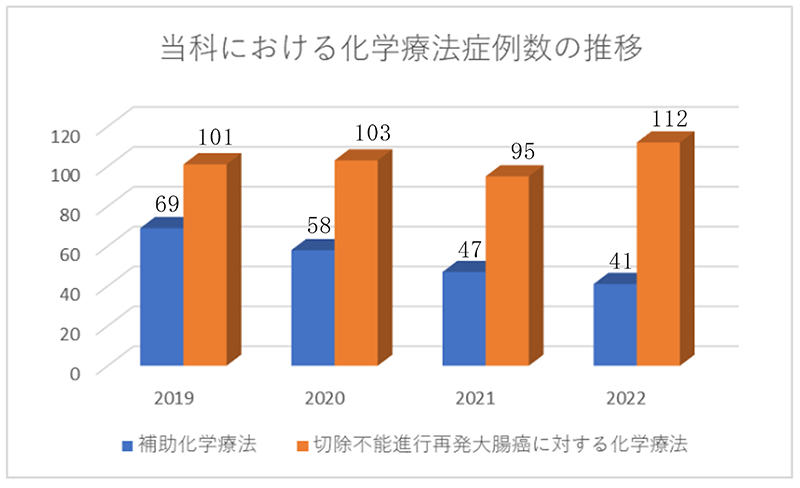
2.切除不能進行・再発癌に対する化学療法の実績
切除不能進行再発大腸癌に対して年間約73例の化学療法を施行しております。
切除不能進行再発大腸癌で最初に使用される化学療法は下記の方法が大腸癌治療ガイドラインで推奨されており当科でも行っています。
First line
•FOLFOX + Bmab
•CapeOX + Bmab
•SOX + Bmab
•FOLFIRI + Bmab
•S-1+IRI + Bmab
•FOLFOX + Cmab / Pmab
•FOLFIRI + Cmab / Pmab
•FOLFOXIRI + Bmab
•Infusional 5-FU + LV + Bmab
•Cape + Bmab
•5-FU + LV + Bmab
•S-1 + Bmab
•UFT + LV + Bmab
MSI-H陽性症例
Pembro
軸となるのは、FOLFOX療法、FOLFIRI療法、CapeOX療法でそれに分子標的薬と呼ばれるPanitumumab、Cetuximab、Bevacizumabを加えるのが基本的な投与方法です。
①FOLFOX療法とは
オキサリプラチン、フルオロウラシル、レボホリナートを組み合わせる療法です。
オキサリプラチンとは、第三世代のプラチナ製剤で、2本のDNA鎖の間に入り込んで、DNAの合成を阻害します。
特徴的な副作用、末梢神経障害。
フルオロウラシルとは、DNAの合成に必要な物質の1つであるウラシルに似た分子構造を持ち、ウラシルの代わりにDNAに取り込まれてその合成を阻害し、抗腫瘍効果を発揮します。特徴的な副作用は下痢、出血性腸炎。
レボホリナートとは、それ自体は抗がん剤ではなく、抗がん剤の副作用軽減や作用増強に用いられる“補助剤”です。
レボホリナートの本質は、栄養成分の1つである“葉酸”です。ヒトは、この葉酸を体内で作り出せないことから、食事によって摂取する必要があります。
1941年に、ほうれん草の葉から発見されたことを受けて、葉酸と呼ばれるようになりました。
②FOLFIRI療法とは
イリノテカン、フルオロウラシル、レボホリナートを組み合わせる療法です。
イリノテカンとは、植物の成分から作られた抗がん剤ですが、がん細胞のDNAの合成を阻止して、がん細胞の増殖を抑制します。
特徴的な副作用は下痢。
③CapeOX療法とは
カペシタビン、オキサリプラチンを組み合わせる療法です。
カペシタビンとは、がん細胞の核酸のDNA形成に必要なピリミジンの合成を阻害します。
特徴的な副作用は手足症候群。
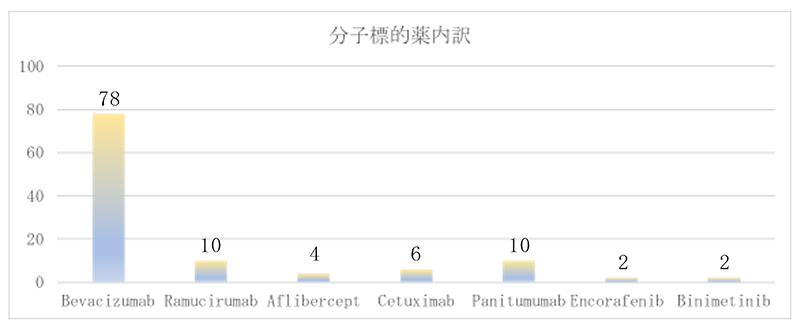
分子標的薬とは
分子標的薬とは、がん細胞の持つ特異的な性質を分子レベルでとらえ、浸潤、転移、増殖に関わる分子を標的として作用するようにつくられた薬です。がん細胞を狙って作用するため、副作用をより少なく抑えながら治療効果を高めると期待されています。
Panitumumab、Cetuximabは、大腸がんの細胞膜の表面にあるEGFRという受容体に結びつく分子標的薬です。
特徴的な副作用は皮膚障害。
Bevacizumabは、がん細胞の血管新生を抑制するために血管内皮細胞増殖因子(VEGF)を阻害する薬で、がん細胞を兵糧攻めにしがん細胞の増殖速度を低下させます。
特徴的な副作用、高血圧、蛋白尿、消化管穿孔、血栓症。
また、全ての標準治療が無効となった患者さんで、全身状態が良好に維持されている場合には、Regorafenib投与が生存期間を延長することが示され、当院でも2013年4月より導入し、19例施行しております。
特徴的な副作用は、手足症候群、高血圧。
また、2014年5月にトリフルリジン・チピラシル塩酸塩が製造販売承認を取得しました。本薬の承認は全世界で日本が最初であり、標準的な治療が困難で治癒切除不能な進行または再発の結腸・直腸癌の治療で新たな選択肢となると期待されています。
当院では2015年に11例施行しました。
特徴的な副作用は消化器症状、骨髄抑制。
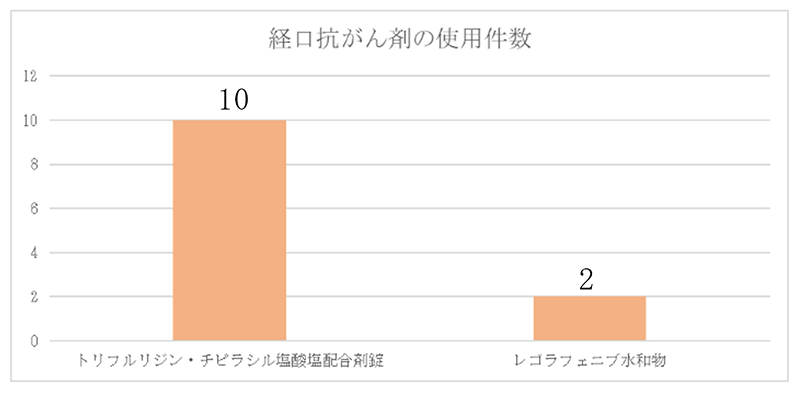
コメント
昨年度は、新型コロナウイルス感染症の影響で化学療法の件数が増えてきていると考えられます。
2022年に大腸癌治療ガイドライン2022が出版されました。
変更された点は、切除不能進行再発癌に対する治療薬としてBRAF遺伝子異常大腸癌に対してencorafenib、binimetinibが適応となり追記され、MSI-H陽性症例に対しては、Pembroが適応となり追記されました。

2022年版の大腸癌治療ガイドライン作成委員会委員長は当科の橋口陽二郎教授です。















